Índice de Contenidos
1. ¿Qué es ISO 13485 Producto Sanitario?
ISO 13485 es una norma internacional para los sistemas de gestión de la calidad sólo aplicable a organizaciones que diseñan y desarrollan, producen, instalan y/o prestan servicio para productos sanitarios.La norma ISO 13485, está basada en la Norma ISO 9001, con el mismo formato y muchos de los requisitos, pero con los requisitos particulares relativos a la “satisfacción del cliente” y la “mejora continua” modificados.
ISO 13485 “Productos sanitarios. Sistemas de gestión de la calidad tiene unos requisitos para fines reglamentarios” y establece que se puede implantar un sistema de gestión en las organizaciones con el objeto de: “Demostrar su capacidad para proporcionar productos sanitarios y servicios relacionados que cumplen de forma coherente requisitos del cliente y requisitos reglamentarios aplicables a los productos sanitarios y a los servicios relacionados”
2. Estructura de la Norma ISO 13485
Se trata de una norma que sigue el formato, estructura y enfoque basado en procesos de la norma ISO 9001, pero especifica requisitos adicionales y no incluye requisitos explícitos para la mejora continua y la satisfacción del cliente,
3. Sistema de Gestión de Calidad
La norma une en ISO 13485 de Equipos Médicos acomoda el modelo fundamentado en procesos ISO 9000 para el ámbito de fabricación de Productos Sanitarios regulados. Tiene como base los conceptos del modelo de proceso ISO 9001 de PHVA Plan, Do, Check, Act - Planificar, Hacer, Verificar, Actuar, y está creado para el cumplimiento legislativo con lo que necesita de más documentación su sistema de gestión de la calidad4. Objetivos ISO 13485
Su objetivo fundamental es definir el conjunto de requisitos regulatorios armonizados dentro del área de los productos sanitarios.Se basa en la norma ISO 9001, básicamente en los requisitos de satisfacción cliente y de mejora continua, pero con cambios para adaptarlos al objetivo que se está regulando.
La norma ISO 9001 una norma internacional para los sistemas de gestión de la calidad en general, por lo tanto, todas las organizaciones pueden implantar un sistema de gestión de la calidad.
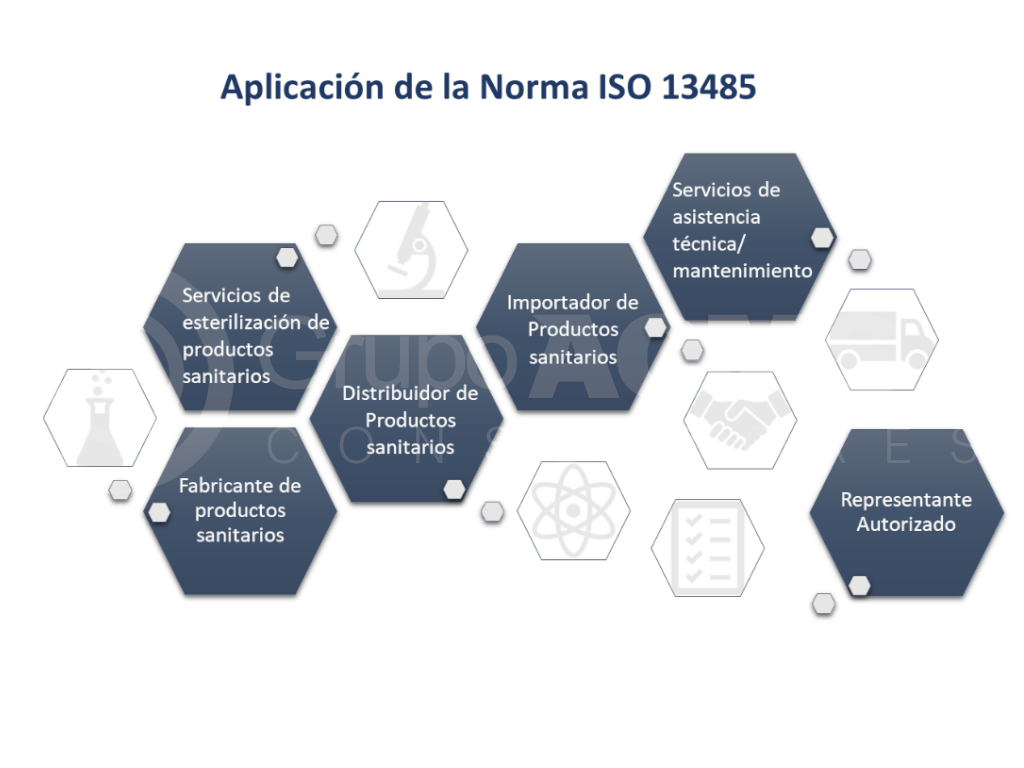
5.¿A quién aplica esta norma?
La norma ISO 13485 de Equipos Médicos se aplica solamente a fabricantes de dispositivos médicos y a sus servicios relacionados, sin tener en cuenta el tamaño o localización .
6. Ventajas
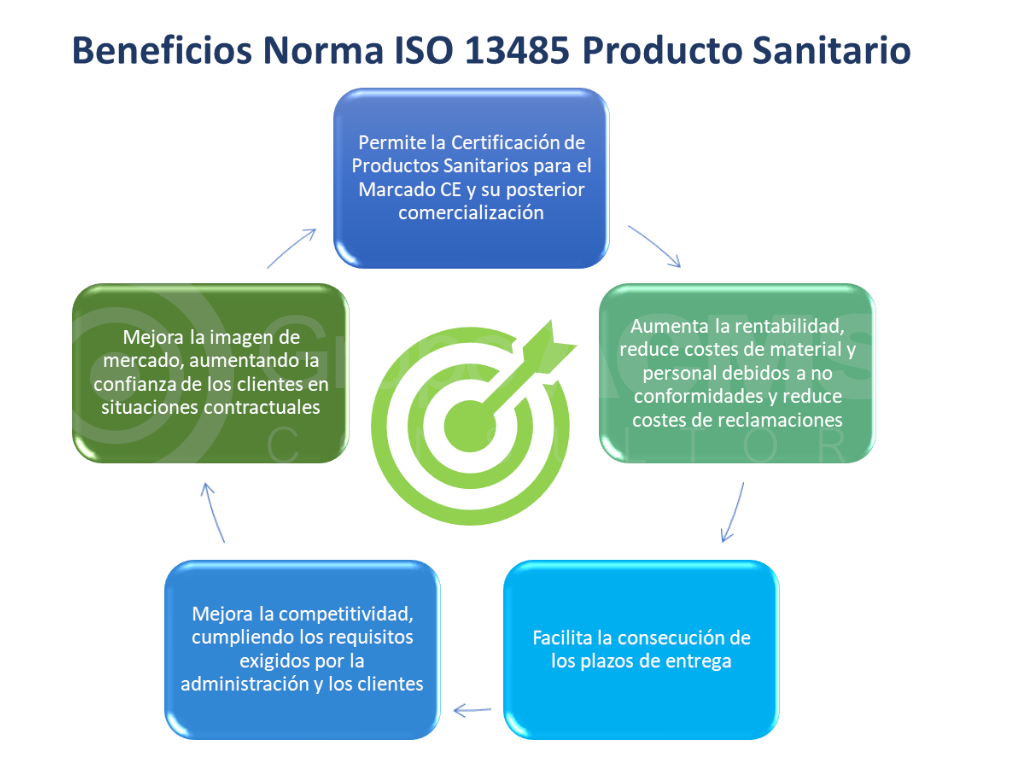
Certificarse en ISO 13485 aporta a las empresas:
- Que los accionistas de la organización se impliquen
- Aumento de la reputación de la marca de empresa
- Clara satisfacción de los clientes
- Ventajas frente a la competencia
 Ampliar Infografía Analítica
Ampliar Infografía Analítica7. Requisitos
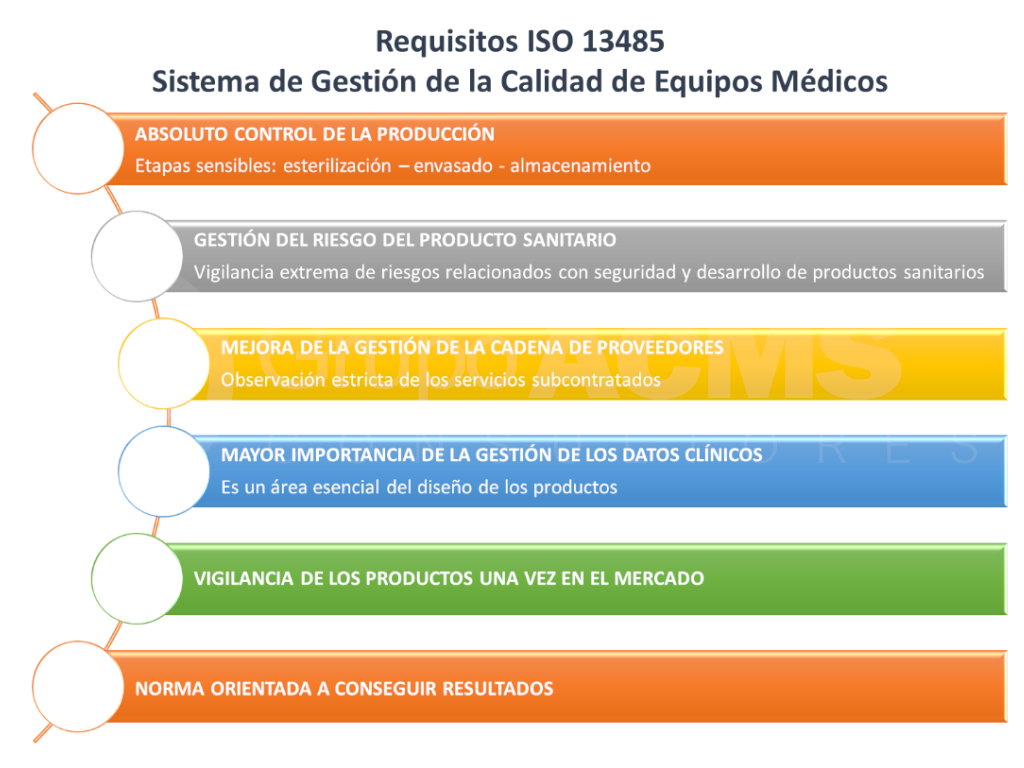
Algunos de los requisitos adicionales que incluye la norma ISO 13485 son:
- Monitorización y control de las condiciones del entorno de trabajo (6.4)
- Diseño y desarrollo (7.3)
- Compras (7.4)
- Actividades del servicio (7.5.1.2.3)
- Validación de los procesos de la producción y prestación del servicio (7.5.2)
- Identificación y trazabilidad (7.5.3)
- Preservación del producto (7.5.5)
- Control de los dispositivos de seguimiento y medición (7.6)
- Verificación del cumplimiento de los requisitos del cliente (8.2.1)
- Análisis de datos (8.4)
- Sistema de Vigilancia (8.5.1)
- Establecer requisitos documentados para las actividades de mantenimiento, y mantener registros de la realización de dichas actividades (6.3)
- Establecer requisitos documentados para la salud, limpieza y vestimenta del personal (6.4)
- Establecer requisitos documentados para las condiciones del entorno de trabajo (6.4)
- Establecer requisitos documentados para la gestión de riesgos en toda la realización del producto, y mantener registros resultantes de la misma (7.1)
- Establecer requisitos documentados para la limpieza del producto (7.5.1.2.1)
- Establecer requisitos documentados para la instalación del producto, y mantener registros resultantes de la misma (7.5.1.2.2)
- En el caso de productos sanitarios estériles, es necesario mantener registros de los parámetros del proceso correspondientes al proceso de esterilización que se utilizó para cada lote de esterilización (7.5.1.3)
- En el caso de productos sanitarios implantables activos y productos sanitarios implantables, al definir los registros necesarios para la trazabilidad, es necesario incluir los registros de todos los componentes, materiales y condiciones del entorno de trabajo (7.5.3.2.2)
- Identificar el estado del producto durante todas las etapas de producción, almacenamiento, instalación y servicio.
 Ampliar Infografía Analítica
Ampliar Infografía Analítica8. Documentación relacionada
Grupo ACMS Consultores puede ayudarle a implementar ambas normas para que obtenga los certificados ISO correspondientes.
Preguntas frecuentes relacionadas
- Código de barras UDI-PI - UDI productos sanitarios
- ¿Quién designa el código UDI o los códigos UDI?
- Fecha límite obligatoria para cumplir con los requisitos UDI
- ¿Quién es el responsable de colocar el código UDI?
- Comercializar un programa considerado producto sanitario



